1问题的提出
现行高二化学课本(人教版)中苯与溴反应的演示实验笔者发现存在以下问题:
(1)实验时由于溴易挥发,有剧毒,造成严重的环境污染,影响了师生健康。
(2)反应不易控制。由于反应物和催化剂一次加入,反应比较剧烈,不易控制反应速率。
(3)产品不易检验。生成的气体中混有一定量的溴蒸气,造成对检验的干扰。
鉴于此,笔者从师生身体健康和教学效果出发,对本实验装置进行了改进。
2实验用品
2mL液溴,4mL苯,CCl4液体,AgNO3溶液,10%NaOH溶液,提拉式铁丝网,脱脂棉,20*200mm 18*180mm具支试管各1支,型管,试管,橡皮塞等。
3实验装置
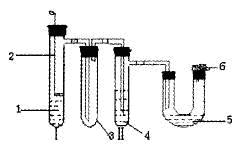
图1 1苯和液溴混合物;2提拉式铁丝网;3安全瓶;4 CCl4液体;5 AgNO3溶液;6吸有NaOH溶液的脱脂棉
4实验操作步骤
(1)检查装置的气密性。
(2)向具支试管倒入4 CCl4液体,向型管中加入AgNO3溶液至弯管处刚好留一小缝隙,在右边导管上放一小团吸有NaOH溶液的脱脂棉,然后再取4mL的苯和2mL液溴倒入具支试管,给具支试管安上橡皮塞,重新连结好装置。
(3)把提拉式铁丝上下拉动几回,使苯和溴混合均匀,然后把铁丝网插入混合液,仔细观察反应过程,1min后无色的四氯化碳由浅黄色到黄色到橙色。同时型管上部有白雾出现,约2min后型管中开始出现淡黄色沉淀生成,约4min反应完毕,型管中有较多的淡黄色沉淀生成,证明产生了溴化氢气体。
(4)反应完毕,把具支试管内液体倒入盛有10mL10%NaOH溶液的小烧杯中,观察到一种棕褐色的油状液体悬浮于烧杯中。振荡!静置,再用水稀释可以看到一种无色油状物即为溴苯。
5实验说明
(1)提拉式铁丝网既是反应催化剂,又能控制反应进程。
(2)苯与液溴开始反应时比较慢,可用30~40度温水浴热一下具支试管。
6实验特点
(1)该实验装置为全封闭装置,药品用量少,基本消除了环境污染。
(2)由无法控制的反应改为可控制的反应,同时排除了液溴对溴化氢中溴检验的干扰。 (3)仪器简单,操作方便,现象明显,安全可靠,整个实验一步到位。 |